Cuando abrimos la heladera accedemos, aun en días calurosos, a helados,
bebidas frías, comidas frescas, hielo o alimentos supercongelados. ¿Cómo
es posible que el interior de la heladera se encuentre tan frío? ¿Qué
hacían las personas para preservar los alimentos cuando no existían las
heladeras?
Aquí encontrarás respuestas a estas preguntas y otros datos interesantes
acerca de la refrigeración, explicados mediante descripciones de fenómenos
físicos elementales y simples acontecimientos cotidianos. En la actividad
se proponen preguntas sobre este texto y dos métodos para medir la humedad
relativa ambiente.
Historia de la heladera
Actualmente es difícil imaginar cómo se arreglaba la gente sin el
refrigerador eléctrico, que apareció hace apenas unos 80 años. Los
antiguos griegos y romanos, por ejemplo, sacaban hielo y nieve de las
cumbres de las montañas, y los guardaban en pozos tapados con madera y
paja donde enfriaban sus alimentos y bebidas. En la Argentina, hasta
mediados del siglo XX, los alimentos se conservaban en armarios cerrados
donde se colocaba diariamente una barra de hielo, que se compraba en las
carbonerías.
Uno de los primeros hechos destacables de la cronología de la
refrigeración aconteció en 1834, cuando Jacob Perkins inventó en
Inglaterra el primer dispositivo para fabricar hielo, basado en un líquido
que se evaporaba y luego se condensaba con la ayuda de una máquina. Poco
después, en 1844, John Gorrie desarrolló en los Estados Unidos una
heladera que funcionaba comprimiendo y expandiendo un gas en forma
alternada. De esta manera se aprovechaba el enfriamiento del gas al
expandirse. En 1920, empezaron a usarse en los Estados Unidos heladeras
eléctricas semejantes a las actuales. El invento se generalizó en la
Argentina varias décadas después. A partir de 1970, se popularizaron los
llamados freezers, que permiten conservar alimentos congelados
en buen estado durante varios meses.
Los principios del funcionamiento de la heladera
El funcionamiento de la heladera se basa en las siguientes propiedades
físicas, que permiten generar frío:
- El calor se transfiere de un cuerpo caliente a uno frío
Para calentar un material debemos acercarlo a una fuente caliente,
que se encuentra a mayor temperatura. ¿Por qué ocurre esto?
La transferencia de calor es un flujo de energía. Cuando se transmite
calor entre dos cuerpos, uno pierde energía y el otro la gana. El
cuerpo que pierde calor disminuye su temperatura o cambia de estado
(por ejemplo, pasa de gas a líquido o de líquido a sólido). Cuando dos
cuerpos a distinta temperatura se ponen en contacto, el calor es
transferido del más caliente al más frío. De esta manera, la
temperatura de ambos tiende a igualarse.
- Los gases muy comprimidos se condensan
Seguramente conocen los encendedores de plástico transparente y
vieron que contienen un líquido. Esos encendedores queman un gas
semejante al que arde en la cocina. Pero ¿dónde está ese gas? El gas
está condensado, es decir, se encuentra en estado líquido, encerrado a
alta presión (comprimido) dentro del encendedor.
Cuando se comprime un gas, el volumen que ocupa se reduce (sus
moléculas se acercan entre sí) y su presión aumenta. Al llegar a una
presión suficientemente elevada (volumen muy pequeño), las moléculas
se acercan lo suficiente como para atraerse entre sí y formar el
líquido.
- La evaporación quita calor
Cuando salimos de la ducha o de la pileta, sentimos frío. ¿Por qué?
El agua, al evaporarse, toma calor, es decir que cuando el agua se
transforma en vapor le quita calor al cuerpo y por eso sentimos frío.
Lo mismo pasa si nos ponemos alcohol o acetona sobre la piel; el
líquido se evapora más rápidamente que el agua, y al quitar más rápido
el calor de la piel sentimos más frío.
En verano mojarse puede ser un alivio. Pero si nos mojamos en
invierno hay que secarse enseguida, porque el agua, al evaporarse,
quita calor del cuerpo. Cuando hace calor o hacemos ejercicio físico,
transpiramos más. La evaporación del sudor ayuda a bajar la
temperatura
del cuerpo.
Esta propiedad también puede observarse con los aerosoles. Cuando
rociamos una cantidad considerable de cualquier producto envasado en
aerosol, notamos que el envase se enfría. ¿Por qué ocurre esto?
- Dentro del envase hay una sustancia, el propelente, que sirve para
impulsar el producto que se desea rociar (por ejemplo, desodorante o
insecticida). El propelente, en condiciones normales, es una
sustancia gaseosa, pero dentro del aerosol se encuentra comprimido
en estado líquido.
- Cuando se oprime la válvula, la presión interna del envase empuja
su contenido hacia fuera y sale el propelente con el producto. Esto
disminuye la presión en el interior del envase.
- Al haber menos presión, parte del líquido que está en el envase se
evapora.
- Al evaporarse, el propelente absorbe calor del ambiente. Por lo
tanto, los materiales próximos, como el envase, se enfrían.
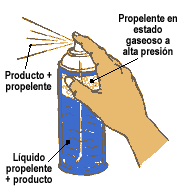
El aerosol se enfría porque la evaporación quita calor.
En los ejemplos anteriores se pudo observar que cuando un líquido se
hace gas (evaporación), quita o absorbe calor. Esto se debe a que el
gas tiene un mayor contenido energético que el líquido, si tienen la
misma temperatura. En el caso contrario, cuando un gas se hace líquido
(condensación), se libera calor. En estas transformaciones, la
diferencia de energía entre ambos es liberada o absorbida en forma de
calor.
- La compresión calienta, la expansión enfría
Cuando inflamos la rueda de una bicicleta, notamos que
el tubo del inflador se calienta. ¿Por qué ocurre esto?
- Cuando un gas se comprime, aumenta su temperatura (se calienta); y
cuando se expande (aumenta su volumen), su temperatura disminuye (se
enfría).
- Al inflar la rueda, empujamos con un émbolo el aire contenido
dentro d el tubo del inflador (le entregamos energía en forma de
trabajo).
- Al comprimirse, el aire aumenta su temperatura, le transfiere
calor al tubo del inflador (que se encontraba a menor temperatura) y
hace que éste se caliente.
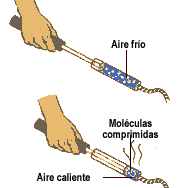
El inflador se calienta porque el gas se comprime.
Estos cambios se deben a la pérdida de energía del gas cuando se
expande, a causa del trabajo que realiza al «empujar hacia fuera» y a
la energía que se le transfiere al comprimirlo cuando se lo «empuja
hacia adentro».
Dentro de la heladera
La temperatura en las diversas zonas de una heladera
La temperatura no es igual en las distintas zonas de la heladera. En el
gabinete principal es de unos pocos grados centígrados sobre cero. En el
congelador es de unos pocos bajo cero y en el freezer es aún más
baja.
Para obtener estas temperaturas, el calor debe fluir desde el interior de
la heladera hacia el exterior. El resultado neto de este proceso es la
transferencia de calor de materiales a menor temperatura (en el interior
de la heladera) a otros de mayor temperatura (en el exterior), lo cual
parece contradecir el principio que dice que el calor se transfiere de un
cuerpo caliente a uno frío. ¿Cómo se logra este efecto?
El proceso cíclico de enfriamiento
El enfriamiento se produce mediante un proceso cíclico en el cual un gas,
como los gases CFC o clorofluorocarbonados, circula por un tubo que
recorre las partes interna y externa de la heladera intercambiando calor.
Los pasos del proceso para producir el enfriamiento son los siguientes.
- Se comprime el gas en una parte de su recorrido que se encuentra en el
exterior de la heladera (el compresor). Entonces aumenta su temperatura
(la compresión calienta).
- Se permite que el gas comprimido y caliente se enfríe (en el
condensador) liberando calor al ambiente (el calor se transfiere de un
cuerpo caliente a uno frío).
- Al enfriarse, el gas comprimido se transforma en líquido (los gases
muy comprimidos se condensan) y libera más calor al ambiente (cuando un
gas se hace líquido libera calor).
- El líquido pasa por un tubo muy delgado (capilar) que impide su
expansión, al sector que se encuentra dentro de la heladera.
- El líquido pasa a un tubo más grueso (evaporador), en la parte
interior, que permite que el líquido se evapore y que el gas formado se
expanda. Estos procesos quitan calor del interior de la heladera (la
evaporación quita calor, la expansión enfría).
- Al perder calor, el interior de la heladera se enfría (el cuerpo que
pierde calor disminuye su temperatura).
- El gas pasa al exterior de la heladera donde vuelve a ser comprimido y
todo el proceso se vuelve a repetir.
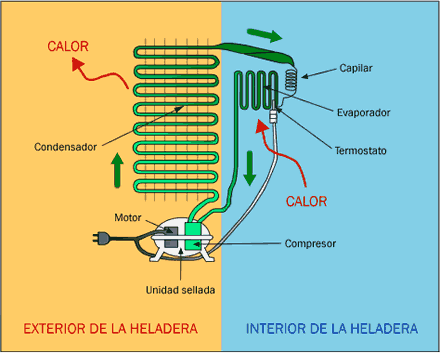
Las partes de una heladera
Las principales partes de una heladera, donde ocurren estos procesos, son
las siguientes.
Motor: toma energía de la instalación eléctrica e impulsa
el compresor.
Compresor: es impulsado por el motor y comprime el gas de
la tubería, calentándolo.
Condensador: parte de la tubería donde se enfría el gas
recién comprimido, que entonces se condensa. Está en el exterior de la
heladera y libera calor al ambiente.
Capilar: tubo que deja pasar poco a poco el gas licuado.
Se lo llama así porque es muy delgado; un tubo grueso dejaría pasar el gas
sin resistencia e impediría la compresión.
Evaporador: tubo sinuoso que está en contacto con lo que
llamamos el congelador de la heladera. En este tubo se evapora el gas
previamente licuado y así se enfría el interior de la heladera. El
evaporador y el congelador se ubican arriba para que el aire frío, más
denso, baje por su propio peso y reemplace el aire más caliente; que sube.
Si el congelador estuviera abajo, el frío llegaría arriba con mayor
dificultad.
Termostato (vulgarmente, «el automático»): mecanismo
automático que interrumpe la corriente eléctrica cuando la temperatura es
suficientemente baja, y pone a andar nuevamente el motor cuando sube la
temperatura.
Unidad sellada (conocida como la «bocha»): recipiente
hermético donde están ubicados el motor y el compresor. Esta disposición,
incorporada hacia 1950, reduce el riesgo de las fugas de gas.
Heladeras sin motor
Heladeras de absorción con amoníaco
Hay heladeras que queman querosén para funcionar. No tienen motor, ni
compresor ni piezas móviles; su principio de funcionamiento es el
siguiente:
- Una pequeña llama hace hervir una solución de amoníaco en agua
(solución fuerte, en el esquema).
- El amoníaco se separa como gas (evaporador) y se reúne con el agua en
otro lugar del circuito (absorbedor).
- El amoníaco gaseoso, al disolverse nuevamente en agua (proceso llamado
absorción), forma una solución (solución débil en el esquema), absorbe
calor y produce el enfriamiento.
- La solución se concentra y se vuelve a calentar.
Este tipo de heladera se usaba mucho en establecimientos de campo que
carecían de energía eléctrica.
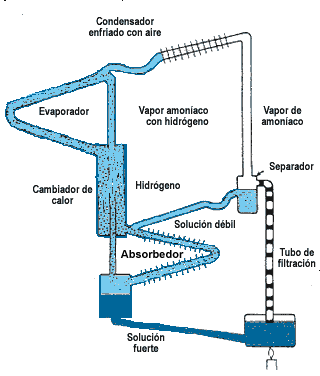
Heladera con amoníaco
Heladeras de termopar
Hay otras heladeras que no tienen piezas móviles ni gases. Utilizan una
unidad que funciona con electricidad, llamada termopar
que transfiere calor entre sus dos caras al circular electricidad. Cuando
una corriente eléctrica atraviesa la unión entre dos conductores
eléctricos de diferente material, la unión se enfría o calienta, según en
qué sentido circule la corriente. Estas heladeras, de termopar, no se
desgastan, no hacen ruido y pueden ser muy pequeñas, por lo que son
ideales para las habitaciones de hotel, donde el ruido del motor de las
heladeras comunes podría incomodar a los huéspedes.
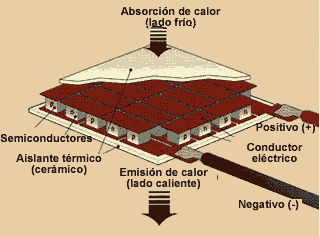
Refrigeración con un termopar
Más datos útiles sobre las heladeras
Algunos datos adicionales sobre las heladeras y su funcionamiento.
- La capacidad de una heladera se mide en pies cúbicos. Aproximadamente
35 pies cúbicos equivalen a un metro cúbico.
- Cuando una heladera marcha casi sin parar y forma mucha escarcha, esto
es señal de que el cierre de la puerta es imperfecto. Hay que ajustarlo
o reemplazar el burlete de goma.
- El agua que se obtiene al descongelar la escarcha contiene pocas
sales, porque proviene de la condensación de la humedad ambiente, que no
las tiene.
- Al congelarse, el agua aumenta su volumen, por eso es peligroso
colocar una botella cerrada en el congelador: si está muy cargada podría
romperse cuando el líquido se congela.
Cronología de la refrigeración
- Antes de 1748. El enfriamiento se efectúa con hielo o nieve.
- 1748. El escocés William Cullen logra por primera vez la refrigeración
artificial por medio de la evaporación de un líquido.
- 1805. El inventor estadounidense Oliver Evans diseña la primera
máquina refrigeradora que usa vapor en vez de líquido.
- 1834. El inglés Jacob Perkins inventa la primera máquina que fabrica
hielo a partir de la evaporación y la condensación de un líquido.
- 1844. El médico estadounidense John Gorrie construye una heladera que
funciona comprimiendo y expandiendo un gas en forma alternada.
- 1856. El empresario estadounidense Alexander Twinning introduce en el
mercado sistemas de refrigeración.
- 1859. El francés Ferdinand Carré utiliza amoníaco en lugar de aire en
los sistemas de refrigeración. De esta manera consiguió temperaturas más
bajas.
- 1920. Se comienza a utilizar el gas freón en lugar del amoníaco.
Escalas de temperatura
Existen varias escalas para medir la temperatura. La de uso más
generalizado para aplicaciones cotidianas es la Celsius o centígrada.
Escala Celsius
Su unidad es el grado Celsius (°C), según la cual a
presión atmosférica normal el agua pura hierve a los 100 °C y se congela a
los 0 °C.
Escala Fahrenheit
La unidad de medida es el grado Fahrenheit (°F). Según
esta escala, el agua hierve a 212 °F y se congela a 32 °F.
Para pasar de grados Fahrenheit (°F) a Celsius (°C), o a la inversa, se
utilizan las siguientes fórmulas:
°C = 5 (°F - 32) / 9
°F = 9 °C / 5 + 32
En los Estados Unidos se utiliza la escala Fahrenheit en aplicaciones
cotidianas.
Una novela de Ray Bradbury (EE.UU., 1920), Fahrenheit 451,
presenta una sociedad del futuro en la que los bomberos no apagan
incendios –no se producen porque las casas son incombustibles–, y se
dedican a quemar libros. El título alude a la temperatura a la que arde el
papel, unos 233 °C.
Escala Kelvin o absoluta
En aplicaciones técnicas y científicas se suele emplear la escala Kelvin
o absoluta, cuya unidad es el kelvin (K). La temperatura
más baja posible en la naturaleza es de unos 273 °C bajo cero; se conoce
como cero absoluto y equivale a 0 K.
Para convertir grados Celsius en kelvin hay que sumar 273 a los grados
Celsius:
K = °C + 273
Por ejemplo, la temperatura de los objetos en el espacio, lejos del calor
de las estrellas, es de unos -270 °C, o 3 K.
Si se baja la temperatura de un gas manteniendo constante su presión, el
gas disminuye su volumen. El cero absoluto es la temperatura a la cual un
gas ideal alcanzaría un volumen nulo. Los gases reales se apartan de este
comportamiento ideal y se transforman en líquidos a bajas temperaturas.
Glosario
Amoníaco: sustancia gaseosa a temperatura ambiente,
formada por moléculas que contienen tres átomos de hidrógeno y uno de
nitrógeno (su fórmula química es NH3). Tiene olor penetrante e
irritante. Es muy soluble en agua, en la que forma hidróxido de amonio,
por lo cual sus disoluciones acuosas son alcalinas.
Energía: poder, capacidad para realizar trabajo.
Frío: propiedad de los cuerpos que tienen baja
temperatura. Enfriar un cuerpo equivale a disminuir su temperatura; para
ello hay que extraerle energía, ya sea en forma de calor o de trabajo que
el cuerpo realice sobre el ambiente.
Temperatura: medida de lo caliente o lo frío que se
encuentra un cuerpo. Está relacionada con la energía cinética o de
movimiento de las partículas atómicas o moleculares que componen la
materia. Cuando aumenta la vibración o el desplazamiento de las moléculas,
aumenta la temperatura.
Freezer (congelador): se utiliza este término
para los congeladores que mantienen los alimentos a una temperatura del
orden de los 18 °C bajo cero, bastante inferior a la del congelador común
de las heladeras. Eso permite conservar alimentos durante meses, porque
los microbios, aunque permanezcan vivos, no se pueden reproducir a una
temperatura tan baja como lo hacen a la temperatura del congelador común.
Clorofluorocarbonados (CFC): sustancias químicas
volátiles formadas por los elementos cloro, flúor y carbono. Se utilizan
en heladeras y sistemas de refrigeración para intercambiar calor, pero
perjudican la atmósfera cuando se escapan: adelgazan la capa de ozono, que
es la que nos protege de las radiaciones peligrosas del sol. A partir del
año 2000, la mayoría de los países cumplirá el acuerdo de reemplazarlos
por otros gases menos perjudiciales para el ambiente.
Bibliografía comentada
- Cerdeira, S., E. Ortí, A. Rela y J. Sztrajman, Física-Química,
Buenos Aires, Aique, 2000.
Libro de texto destinado a la enseñanza media. En la página 120 hay un
juego para comprender el mecanismo de propagación del calor por
conducción. Sólo se requiere saber sumar y dividir por 2.
- Macaulay, D. y N. Ardley, Cómo funcionan las cosas, Buenos
Aires, Editorial Atlántida, 1994.
Obra útil para saber cómo funcionan los objetos que utilizamos a diario.
La sencillez de las explicaciones la hacen especialmente apropiada para
los niños.
- Rela, A., Física y artefactos domésticos, Buenos Aires,
Editorial Angström, 1994.
Obra en la que se encuentran muchas curiosidades y ejemplos hogareños.
El docente los puede relacionar con los contenidos y adaptarlos según
los niveles de enseñanza. Incluye una prueba de conocimientos para
detectar preconceptos.
Enlaces a sitios de interés
Historia
y curiosidades sobre la heladera (en inglés).
Descripción
del funcionamiento de la heladera.






