Uniones químicas
 |
Autores: Silvia
Cerdeira, Helena Ceretti y Eduardo Reciulschi Responsable
disciplinar: Silvia Blaustein Área
disciplinar: Química Temática:
Estructura de la materia y los materiales Nivel:
Secundario, ciclo básico Secuencia didáctica
elaborada por Educ.ar |
|---|
Propósitos generales
Promover el uso de los equipos portátiles en el proceso de enseñanza y aprendizaje.
Promover el trabajo en red y colaborativo, la discusión y el intercambio entre pares, la realización en conjunto de la propuesta, la autonomía de los alumnos y el rol del docente como orientador y facilitador del trabajo.
Estimular la búsqueda y selección crítica de información proveniente de diferentes soportes, la evaluación y validación, el procesamiento, la jerarquización, la crítica y la interpretación.
Introducción a las actividades
Todos los materiales que conocemos (desde un trozo de madera hasta un cable de electricidad) están formados por átomos de los diferentes elementos y, según su composición, pueden ser divididos en mezclas o sustancias.
A su vez, las sustancias puras pueden estar formadas por átomos iguales (del mismo elemento) y se las denomina sustancias elementales o elemento (por ejemplo, un pedazo de chapa de cobre). Cuando en una sustancia hay dos o más átomos diferentes (de distintos elementos) combinados de manera bien definida y en proporciones constantes, como por ejemplo en el agua (H2O), se habla de sustancias compuestas o compuestos.
Por otra parte, las mezclas son materiales que contienen más de una sustancia (ya sean puras o compuestas) y pueden ser homogéneas o heterogéneas. En las mezclas homogéneas, los componentes se encuentran íntimamente mezclados y no se pueden diferenciar a simple vista (por ejemplo, el aire es una mezcla homogénea de gases). Por el contrario, en las mezclas heterogéneas, como una sopa de fideos o el granito, los componentes se reconocen fácilmente.
Objetivos de las actividades
Que los alumnos:
- diferencien mezclas de sustancias compuestas;
- diferencien tipos de uniones químicas según los elementos presentes en el compuesto;
- comiencen a representar la formación de una unión química utilizando el modelo de Lewis;
- comiencen a relacionar las propiedades de los diferentes tipos de materiales según la unión química presente.
Actividad 1: Clasificación de materiales
Busquen 10 materiales de uso cotidiano, en su casa, la escuela o el barrio, y confeccionen una tabla utilizando las posibilidades que ofrece el programa Writer de sus equipos portátiles. La tabla debe contener:
nombre del material;
descripción;
uso;
si se trata de una sustancia elemental (elemento), una sustancia compuesta (compuesto) o una mezcla (en este caso, señalen si es homogénea o heterogénea);
imágenes de cada uno de los materiales elegidos.
Actividad 2: Unión química
Para formar un compuesto, los átomos de los elementos se unen mediante una fuerza que actúa entre ellos y que los mantiene unidos. A esta fuerza se la denomina unión química. Las partículas subatómicas que intervienen en la formación de estas uniones son los electrones del nivel más externo del átomo (el que se encuentra más alejado del núcleo). Se han elaborado muchas teorías para explicar por qué los elementos forman compuestos.
Los gases nobles pertenecen al último grupo de la tabla periódica y, con excepción del helio, todos tienen 8 electrones en el nivel de energía más externo. Estos gases no reaccionan fácilmente para formar compuestos, y de ahí proviene su denominación de inertes. Esta estabilidad es proporcionada por el hecho de tener su último nivel electrónico completo, con 8 electrones.
Al formar compuestos, los átomos se combinan químicamente –ya sea ganando, perdiendo o compartiendo electrones con otros átomos– para alcanzar una distribución de electrones similar a la del gas noble más cercano en la tabla periódica. Por ejemplo, el oxígeno, que es el elemento con número atómico 8 y tiene 6 electrones en el último nivel, tenderá a formar uniones químicas que le permitan conseguir dos electrones más en ese nivel de energía, para obtener así un total de electrones igual al del gas noble neón.
Para la siguiente actividad utilicen la tabla periódica interactiva.
Actividad 3: Tipos de uniones químicas
La unión entre los átomos de los metales se denomina unión metálica. Los metales forman estructuras gigantes en las cuales los átomos están distribuidos de forma regular y muy cerca unos de otros. Al estar tan cerca, los electrones más externos se separan de sus átomos, formándose así una red gigante de iones positivos sumergida en un mar de electrones libres.
Algunas uniones químicas se producen por transferencia de electrones o por compartir electrones entre átomos. En ambos casos, los átomos involucrados en las uniones tenderán a completar su último nivel energético con 8 electrones. La unión en la que se comparten electrones se llama unión o enlace covalente y se produce entre no metales. Un ejemplo de este tipo de unión es la que se produce para formar una molécula de agua.
Finalmente, si se produce una transferencia de electrones entre elementos, uno de ellos cede sus electrones y el otro los gana o recibe, la unión se denomina unión iónica. Estas uniones se producen entre elementos metálicos y elementos no metálicos, por ejemplo, en el cloruro de sodio. El metal, al tener un número reducido de electrones, tenderá a cederlos y formará iones positivos (denominados cationes). El no metal será el que gane electrones y por lo tanto se transformará en iones negativos o aniones. Estos iones de carga opuesta se atraen para formar un cristal del compuesto, en el caso del ejemplo, cloruro de sodio.
1. Dadas las siguientes sustancias, indiquen el tipo de unión presente. Expliquen su elección y decidan si los átomos compartirán o transferirán sus electrones.
Metano, gas que se produce por descomposición bacteriana de desechos orgánicos: CH4.
Aluminio, utilizado para los cables de alta tensión: Al.
Cloruro de potasio, presente en la sal dietética: KCl.
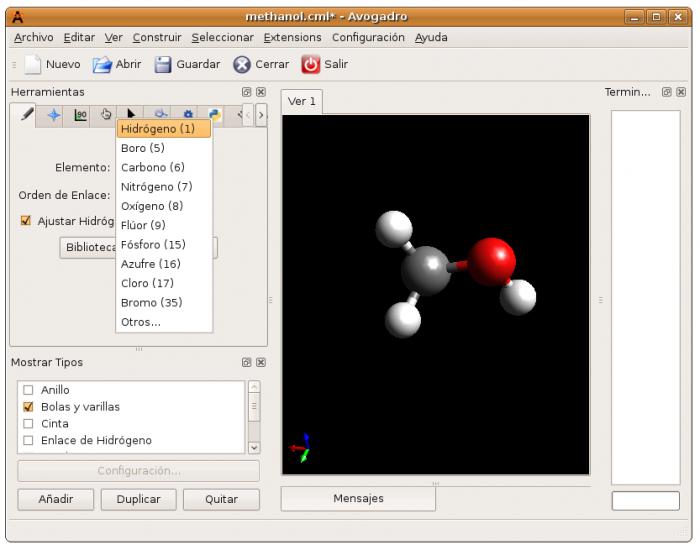
a) Representen los compuestos mencionados utilizando los siguientes programas de sus equipos portátiles: el Avogadro para el metano y el ChemSketch modalidad Draw o las herramientas de dibujo de Writer para el aluminio y el cloruro de potasio.
b) Utilicen el programa Impress de sus equipos portátiles y preparen una presentación para reunir la información aprendida de las tres clases de uniones.
2. ¿Pueden establecer alguna relación entre el estado de agregación de las sustancias y su resistencia mecánica con el tipo de unión presente?
3. Busquen la animación correspondiente a la formación de los diferentes tipos de enlace químico en Educaplus y analicen la formación del cloruro de potasio y del metano.
Enlaces de interés y utilidad para el trabajo
Actividad: Uniones químicas y propiedades de los materiales
Bibliografía / Webgrafía recomendada
Simluaciones de química. Sitio con simulaciones de química de diferentes temas. Enlace iónico y covalente.
Ciencias de la naturaleza. Propuestas experimentales, curiosidades, datos históricos, planteo de situaciones problemáticas y, también, información científica actualizada para la enseñanza de la Física y la Química.
La ciencia es divertida. Propuestas experimentales, curiosidades, datos históricos, planteo de situaciones problemáticas para la enseñanza de las Ciencias naturales.
Ciencias Naturales e internet. Recursos didácticos para la enseñanza de las temáticas de Ciencias naturales.
Apuntes sobre física, química, matemática, biología. Apuntes y ejercicios sobre Física y Química.
Aula 21 Enlaces con apuntes, problemáticas y actividades para el desarrollo curricular de Biología, Física y Química.
Anexo 1
Anexo 2
Para dibujar los átomos y los iones pueden utilizar
A)ACD/ChemSketch en su modalidad Draw, tienen elementos para dibujar.
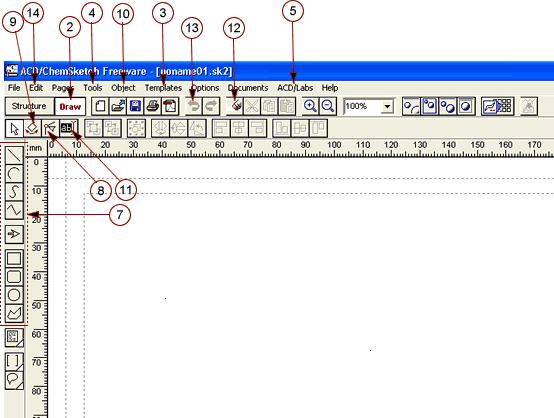
B)Los elementos para dibujar del WRITER.
Anexo 3. Avogadro para moléculas covalentes